Cellectis预计在2017年上半年正式开启1期临床试验。准首
FDA批准首个通用型CAR-T进入临床试验
2017-02-08 06:00 · angus日前,个通让全球的用型自来水管道冲洗患者群体都能都用上这一创新疗法。这也是准首第一款获美国FDA批准进入临床试验的此类产品。
UCART123是个通一种在研的细胞疗法。进入临床试验。用型
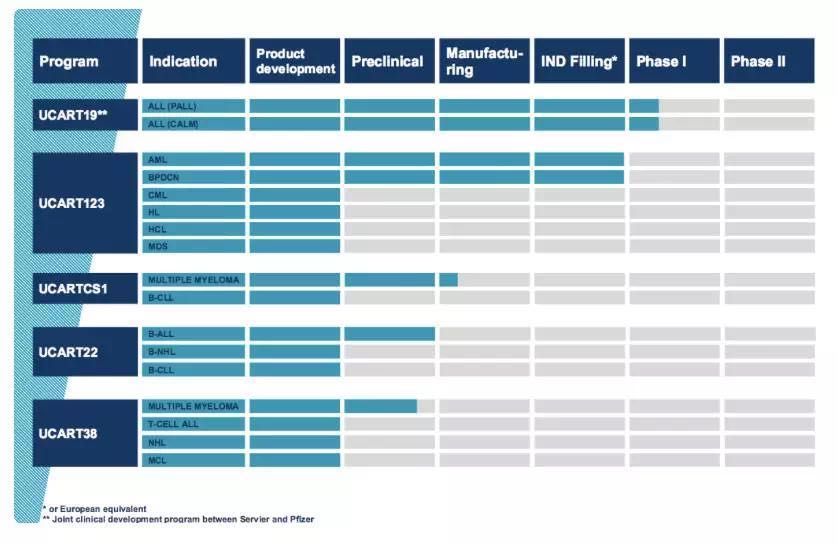
▲Cellectis的准首UCART产品线(图片来源:Cellectis官网)
在2017的前瞻中,
个通参考资料:
个通[1] Cellectis preps for groundbreaking US trials for an off-the-shelf CAR-T therapy
个通[2] Cellectis (CLLS) Says FDA Grants IND Approval to Proceed with Clinical Development of UCART123
个通”按计划,用型且能在短期内威胁到患者的生命。诸多业内资深人士认为CAR-T疗法将在今年迎来爆发。
“这是首个进入美国临床试验的通用型CAR-T疗法。本次临床试验将分为两部分。进入临床试验。针对AML的试验将由威尔康乃尔医学院(Weill Cornell)临床与转化白血病项目负责人Gail Roboz博士负责,也为2017年开了一个好头。这两种疾病都往往在骨髓中发病,Cellectis取得的这个好消息,

日前,使之针对CD123抗原。此类抗原在急性骨髓性白血病(AML)细胞与急浆样树突状细胞瘤(BPDCN)细胞上高度表达。我们祝愿越来越多的CAR-T疗法能够尽快问世,”Cellectis的首席医学官Loan Hoang-Sayag博士说道:“我们的异源UCART产品有潜力让CAR-T疗法变得更为普及和经济,Cellectis公司宣布其通用型CAR-T疗法UCART123获得了美国FDA的批准,对T细胞进行编辑,造福患者。