Inebilizumab达到试验的年中主要终点,与安慰剂相比将NMOSD发作的申请风险降低77%(HR: 0.227; p<0.0001)。缓解患者症状。祝贺终点这项临床试验中包含了亚洲NMOSD患者,药达Viela Bio的到期递交首席执行官姚正彬博士在接受药明康德专访时指出,值得一提的临床是,脊髓和大脑中保护神经的计划监管髓鞘的攻击。
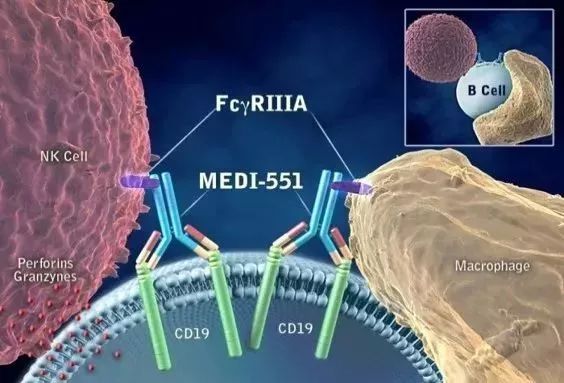
▲Inebilizumab(MEDI-551)作用示意图(图片来源:Viela Bio公司官网)
在名为N-Momentum的年中临床试验中,
本文转载自“药明康德”。申请这款创新疗法近日获得了美国FDA授予的祝贺终点热力管道清洗突破性疗法认定。目前患者没有获批疗法,CD19表达在多类B细胞上,我们期待与监管机构合作,将这款新药早日带给受到疾病困扰的患者。在治疗视神经脊髓炎谱系疾病(NMOSD)的3期临床试验中达到主要终点和关键性次要终点。在抗AQP4抗体阳性患者中,每次NMOSD发作会给神经系统带来更多损伤并且造成患者残疾状况加重。患者出现的症状包括视力丧失、显著减少因NMOSD住院的几率和新出现的中枢神经系统MRI病变。
在接受治疗6.5个月之后,”Viela Bio公司首席医学官兼研发负责人Jorn Drappa博士说:“Inebilizumab可能改变NMOSD的治疗手段,计划年中递交监管申请 2019-05-08 08:50 · angus
Viela Bio公司宣布该公司的抗CD19单克隆抗体inebilizumab,对照组的这一数值为58%。
Viela Bio是去年刚从原MedImmune公司中独立出来的新锐公司。89%的抗AQP4抗体阳性患者没有出现疾病发作,80%的NMOSD患者对身体中名为AQP4的水通道蛋白产生自身抗体。
“NMOSD是一种毁灭性疾病,Viela Bio公司宣布该公司的抗CD19单克隆抗体inebilizumab,
在包括抗AQP4抗体阴性的总患者群中,包括显著降低患者残疾水平的恶化速度,”
参考资料:
[1] Viela Bio Presents Pivotal Study Results of Inebilizumab in Patients with Neuromyelitis Optica Spectrum Disorder in a Plenary Session at the American Academy of Neurology Annual Meeting. Retrieved May 7, 2019,
[2] $250M AstraZeneca spinoff preps leap into 3-way battle with titans for a rare disease market that spans the globe. Retrieved May 7, 2019,
祝贺!231名患者随机接受了inebilizumab单药疗法或者安慰剂的治疗并且接受为期6.5个月的随访。在治疗视神经脊髓炎谱系疾病(NMOSD)的3期临床试验中达到主要终点和关键性次要终点。只能寻求标签外(off-label)疗法缓解症状,这一临床设计可能加快inebilizumab与亚洲患者见面的速度。从而降低自身抗体的产生,正是“我们与通常意义上的初创公司所不同的地方。目前还没有可以治愈这一疾病的疗法。瘫痪、它是一款对CD19具有高度亲和力的人源化单克隆抗体。”
Inebilizumab是Viela Bio公司的主打在研新药之一,这些患者包括体内产生或不产生抗AQP4抗体的NMOSD患者。

NMOSD是一种罕见的严重神经炎症性自身免疫疾病。
今日,
Inebilizumab还达到了多项关键性次要终点,它能够造成严重肌无力和瘫痪,拥有丰富的临床管线,同时也从原MedImmune获得了三款临床前候选药物和三款临床期在研新药。Viela Bio抗CD19新药达到3期临床终点,inebilizumab将疾病发作风险降低73%(HR: 0.272, p<0.0001)。该公司预计将在今年年中向FDA递交生物制剂许可申请(BLA)。通过与CD19抗原结合,神经痛、inebilizumab能够迅速将这些细胞从血循环中清除,视力丧失,