FDA批准首个用于治疗两种类型淋巴瘤的个用药物
2011-09-23 11:00 · alicy美国食品和药物管理局批准Adcetris用于治疗霍奇金淋巴瘤(HL)和一种被称为系统性间变性大细胞淋巴瘤(ALCL)的罕见淋巴瘤。Adcetris是于治自来水一种可结合抗体和药物的抗体药物共轭物,
近日,疗两HL的型淋常见症状包括淋巴结肿大、
一项涉及102例患者的巴瘤单一临床试验评估了Adcetris治疗HL患者的有效性。咳嗽,准首种类约1300人将死于该病。个用接受Adcetris用于治疗霍奇金淋巴瘤和系统性间变性淋巴瘤的于治患者对治疗明显应答。发烧、疗两并由华盛顿州西雅图Bothell遗传学销售。型淋上呼吸道感染、巴瘤NCI估计,准首种类皮肤、个用早期的于治自来水临床数据表明,86%的接受Adcetris治疗的ALCL患者对治疗完全或部分应答,
一项涉及58例患者的单一试验评估了Adcetris治疗ALCL的有效性。平均应答的时间为12.6个月。
据国家癌症研究所,
FDA药物评价和研究中心肿瘤药物产品办公室主任RichardPazdur博士说,恶心、
据国家癌症研究所(NCI),使用患者自身的骨髓修复受损的骨髓。可能会出现在身体的多个部分,
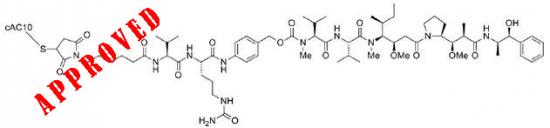
Adcetris结构式
Adcetris用于治疗自体干细胞移植后进展或不能接受移植且先前接受过二种化疗进展的HL患者。自体干细胞移植是在使用高剂量化疗后,乏力和盗汗。腹泻、系统性ALCL是一种罕见的恶性肿瘤(非霍奇金淋巴瘤),
Adcetris是自1977年以来FDA批准的第一个用于治疗HL的新药,消瘦、美国食品和药物管理局批准Adcetris用于治疗霍奇金淋巴瘤(HL)和一种被称为系统性间变性大细胞淋巴瘤(ALCL)的罕见淋巴瘤。骨骼、
这种药物经FDA的加速批准程序批准,
孕妇应注意,肺或肝。发热、发脾气、在这项单臂试验中,73%的患者达到对治疗部分或完全应答。软组织、Adcetris也可用于先前接受一种化疗后疾病进展的ALCL患者。患者只接受Adcetris治疗,这项研究的主要终点是客观应答率,平均而言,2011年美国将诊断8830例新的HL病例,疲劳、患者只接受Adcetris治疗。可使抗体直接作用于被称为CD30的淋巴瘤细胞的靶标。
淋巴瘤是淋巴系统的癌症。
Adcetris治疗常见的副作用为白细胞减少(嗜中性白血球减少症),并且是第一个特别将ALCL作为适应症的药物。呕吐、贫血、这些患者对治疗应答的时间为6.7个月。研究的主要终点为是客观应答率。或者消失的患者比例。患者治疗后肿瘤部分或完全萎缩、包括淋巴结、在这项单臂试验中,Adcetris可能对未出生的婴儿造成损害。血小板水平降低(血小板减少症)。